Les arthropodes des sols dans les cultures de blé : une dominance des prédateurs et des détritivores
Les champs de blé sont un écosystème dans lequel de nombreux arthropodes interagissent entre eux et leur milieu et contribuent à la réalisation de fonctions nécessaires pour la santé des sols et des plantes, telles que la régulation des ennemis des cultures ou le maintien de la fertilité. Mieux les connaître est indispensable à la transition agroécologique en vue de la réduction des intrants de synthèse. Dans cet article, nous faisons un état des lieux des familles d’arthropodes qui peuplent le sol des cultures de blé et de leur rôle dans cet écosystème.

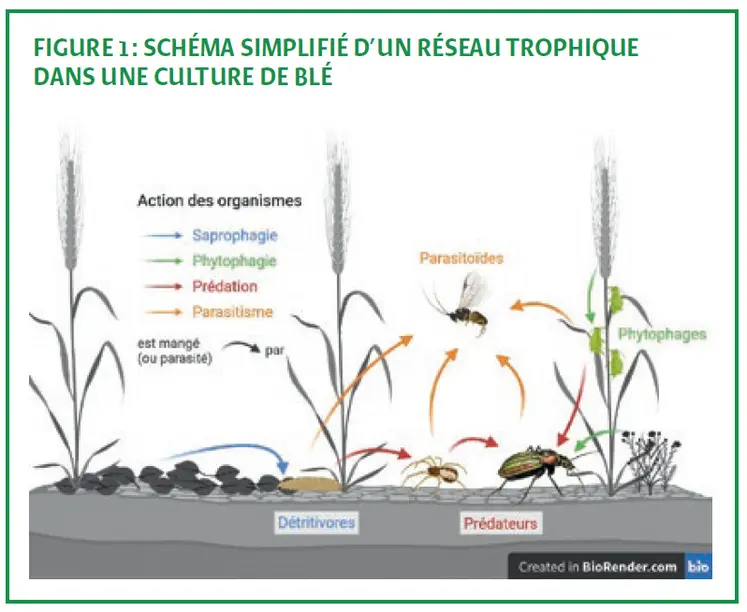
Dans tout écosystème, les êtres vivants sont intégrés dans une chaîne alimentaire. Quatre grands groupes fonctionnels sont définis selon le mode d’alimentation : les phytophages, les détritivores, les prédateurs et les parasitoïdes. Les arthropodes sont des représentants majeurs de ces groupes dans les cultures de blé (figure 1). Les phytophages consomment tout ou partie d’une plante. Ils sont nuisibles s’ils s’attaquent aux cultures (les ravageurs), mais bénéfiques quand ils régulent les adventices et qu’ils pollinisent les autres plantes (les auxiliaires). Les détritivores fragmentent la matière organique morte, facilitant sa décomposition par les micro-organismes. Cela a pour effet d’enrichir le sol en éléments nutritifs. Les prédateurs régulent les populations en consommant d’autres organismes. Ils peuvent jouer un grand rôle dans le contrôle des ravageurs, mais peuvent aussi parfois entraver cette régulation en consommant d’autres prédateurs. Les parasitoïdes pondent à proximité ou dans des individus vivants et leurs larves se développent à l’intérieur de l’hôte, entraînant sa mort. Ils participent aussi à la régulation des populations. Dans cette étude, nous avons identifié les organismes qui contribuent à ces fonctions en champ de blé. Pour cela, nous utilisons des échantillonnages d’arthropodes réalisés en 2019 à l’occasion d’une étude qui a permis d’évaluer l’influence du labour profond et des TCS sur le service écosystémique de régulation assuré par les coléoptères carabiques. La composition des communautés des autres arthropodes capturés dans les pièges a été déterminée à l’échelle de la famille.
Matériel et méthode
L’échantillonnage a été réalisé sur cinq sites du bassin rennais (35) de mars à juillet 2019 dans des cultures de blé d’hiver. Les arthropodes capturés sont des insectes, des arachnides et des myriapodes (mille-pattes). Chaque site comprenait un couple de parcelles dont l’une subissait un labour profond et l’autre un travail du sol superficiel, soit 10 parcelles au total. Pour chaque parcelle, un dispositif identique de capture a été installé. Afin de capturer les individus émergeant du sol, quatre tentes à émergence hermétiques de 60 x 60 cm ont été installées. Elles étaient munies d’un piège Barber (c’est-à-dire un pot enfoui dans le sol) et d’un pot en hauteur pour saisir les individus émergents rampants et volants. Afin de capturer les individus circulant sur la parcelle (émergeant localement, mais également en provenance de l’extérieur du champ), deux autres pièges Barber ont été installés de part et d’autre de chacune des tentes. En complément de ce dispositif, 24 pièges collants étaient disposés dans chaque parcelle pour capturer les collemboles (des petits arthropodes détritivores) au cours de trois sessions en mars, avril et juin.
Composition des groupes fonctionnels
Les 29 629 individus récoltés dans les pièges extérieurs et les tentes à émergence appartenaient à 118 familles. Par ailleurs, 17 647 collemboles ont été capturés dans les pièges collants (tableau ci-contre).
Les phytophages
Les phytophages appartenaient à 30 familles d’arthropodes. Les captures sont les plus abondantes en avril et en juin, lors de la phase de dispersion des adultes. Les phytophages les plus nombreux sont des ravageurs de cultures, dont la famille principale est celle des Aphididae (pucerons). En juin, les effectifs de pucerons explosent. Ce sont essentiellement des individus ailés en quête de nouvelles plantes hôtes. 94 % des individus provenaient de trois pieds de blé présents dans le dispositif de capture. Cette observation est cohérente avec nos connaissances, bien que notre méthode de piégeage ne soit pas adaptée à la capture de ce groupe taxonomique. Les autres phytophages sont les Opomyzidae, des diptères dont les larves mangent l’épiderme des feuilles, les Anthomyiidae et les Elateridae (taupins) qui s’attaquent aux racines, les Cecidomyiidae et les Chrysomelidae qui consomment différentes parties de la plante selon l’espèce. D’autres phytophages ont plutôt une action positive en s’attaquant aux adventices comme les Delphacidae (hémiptères). La pollinisation est, quant à elle, assurée par les hyménoptères de la famille des abeilles (Andrenidae, Apidae, et Melittidae) ou encore les Phalacridae qui sont de minuscules coléoptères. Mais ce rôle est aussi joué par les adultes de nombreuses familles de diptères dont les larves sont tantôt détritivores tantôt ravageuses.
Les détritivores
Ce groupe fonctionnel est majoritairement composé de collemboles, mais comprend aussi 34 autres familles, essentiellement des diptères, des coléoptères et deux myriapodes (mille-pattes). Certains taxons ont un régime alimentaire spécifique. Les collemboles, les Chironomidae et les Polydesmidae sont des saprophages, s’alimentant des résidus de végétaux ; les Lathridiidae et les Lonchopteridae sont des mycétophages, mangeurs de champignons ; les larves de Calliphoridae et Phoridae sont nécrophages et apprécient donc les cadavres et les Aphodiidae sont spécialisés dans la consommation d’excréments et bénéficient probablement des apports en fumier ou en lisier. Les Leiodidae, les Sciaridae et les Sphaeroceridae ont un régime moins spécialisé qui dépend des espèces. Les captures des détritivores augmentent jusqu’en avril, puis diminuent avant d’atteindre un nouveau pic en juillet. Les cortèges diffèrent dans le temps : les coprophages se dispersent en mars-avril tandis que les nécrophages sont capturés en juin-juillet, leur présence indiquant probablement une mortalité plus importante des arthropodes en fin de saison. Chez les saprophages, les émergences se succèdent de manière chronologique selon l’ordre suivant : chironomes- myriapodes-sciaridés. Les détritivores représentent la moitié des individus capturés et constituent une ressource alimentaire importante pour les prédateurs.
Les prédateurs
Les prédateurs comprennent 39 familles dont quatre prédominent : les Carabidae et les Staphylinidae, deux coléoptères, les Linyphiidae, des petites araignées tissant des toiles à proximité du sol et les Lycosidae dénommées aussi araignées loup et chassant au sol. La littérature abonde sur ces familles d’arthropodes bien connues pour leur rôle dans la régulation des ravageurs. Ils peuvent consommer des pucerons, des thrips ou encore des acariens qu’ils recherchent de manière active. Les plus grosses espèces sont opportunistes. Elles peuvent s’attaquer à différentes proies : escargots, limaces, mais aussi vers de terre, détritivores et même d’autres prédateurs. Le groupe des carabes est le plus éclectique, comptant notamment des granivores tels que les Amara et les Harpalus. Les captures de carabes et de staphylins augmentent au cours de la saison ; quant aux araignées, elles sont plus tardives, peut-être parce qu’elles nécessitent plus de chaleur pour éclore et être actives. Les prédateurs représentent un des groupes majeurs avec un tiers de la population capturée.
Les parasitoïdes
Le mois de juillet est le plus propice aux parasitoïdes. Chaleur et abondance en ressources, hôtes et floraison favorisent cette vague d’émergence. Sur les 18 familles, 15 sont des hyménoptères. Les adultes se nourrissent de pollen et participent à la pollinisation. En revanche, les larves sont carnivores et mangent leur hôte de l’intérieur. Ils sont très spécialisés ; ainsi une espèce de parasitoïde est souvent spécifique à une ou quelques espèces d’hôte. Certaines espèces de Braconidae et de Ceraphronidae pondent dans des pucerons ; les Diapriidae recherchent activement les pupes de diptères ; les Scelionidae sont parmi les plus petits parasitoïdes et apprécient les oeufs d’insectes et de petites araignées ; d’autres s’attaquent à plus gros comme les Ichneumonidae et les Protoctrupidae n’hésitant pas à déposer leur progéniture dans des chenilles ou des coléoptères.
Les effets de la pratique culturale
L’effet de la pratique culturale est significatif pour trois taxons : les staphylins, les carabes et les collemboles (figure 2). Le labour profond favorise les staphylins et réduit les populations de carabes et collemboles. De nombreuses espèces de staphylins ont une taille inférieure à 10 mm. Or, le labour a peu d’impact sur les espèces de petite taille et peut même avoir pour effet de remettre en surface des individus qui étaient enfouis profondément dans le sol. Mais le labour a aussi pour effet de déstructurer le sol et d’enfouir la matière organique, ce qui induit une diminution de la ressource facilement accessible pour les détritivores. Les populations de collemboles sont effectivement bien plus présentes dans les parcelles non labourées que dans les parcelles labourées, notamment en début de printemps. Les collemboles sont une proie pour les carabes, ce qui pourrait expliquer en partie les effectifs moins importants de ces prédateurs dans les parcelles labourées. Les larves de carabes passant l’hiver dans le sol de la culture peuvent également souffrir de mortalité directe due à l’action mécanique du labour.
Conclusion
Cette étude complète les connaissances acquises sur les communautés animales de nos espaces cultivés (arthropodes, mollusques, oiseaux, etc.). Elle a montré que les cultures de blé constituaient un écosystème dans lequel les prédateurs et les détritivores sont les arthropodes majeurs de la vie au sol et que le labour a une influence tantôt positive (staphylins), tantôt négative (carabes et collemboles) sur les familles d’arthropodes les plus abondantes. La pratique culturale influence donc directement et indirectement les processus de régulation du vivant et les mécanismes de recyclage de la matière organique.
Yann Laurent1, Manuel Plantagenest1, Ambre Saccomartret De Preville2, Céline Condachou1, Sebastien Ortiz Martinez2 et Elsa Canard2











